Conteúdo
O que são oncogenes?
Um oncogene é um gene celular cuja expressão provavelmente promove o desenvolvimento de câncer. Quais são os diferentes tipos de oncogenes? Por quais mecanismos eles são ativados? Explicações.
O que é um oncogene?
Um oncogene (do grego onkos, tumor e genos, nascimento), também chamado de proto-oncogene (c-onc), é um gene cuja expressão pode conferir um fenótipo canceroso em uma célula eucariótica normal. Na verdade, os oncogenes controlam a síntese de proteínas que estimulam a divisão celular (chamadas oncoproteínas) ou inibem a morte celular programada (ou apoptose). Oncogenes são responsáveis pela proliferação celular descontrolada predispondo ao desenvolvimento de células cancerosas.
Os oncogenes são divididos em 6 classes que correspondem respectivamente às oncoproteínas que codificam:
- fatores de crescimento. Exemplo: o proto-oncogene que codifica proteínas da família FGF (Fibroblast Growth Factor);
- receptores de fator de crescimento transmembrana. Exemplo: o proto-oncogene erb B que codifica o receptor EGF (Fator de Crescimento Epidérmico);
- Proteínas G ou proteínas de membrana que se ligam ao GTP. Exemplo: proto-oncogenes da família ras;
- membrana tirosina proteína quinases;
- proteínas quinases de membrana;
- proteínas com atividade nuclear.Exemplo: proto-oncogenes Erva A, fos, Junho et c-myc.
Qual é o papel dos oncogenes?
A renovação celular é garantida pelo ciclo de célula. Este último é definido por um conjunto de eventos que geram duas células-filhas a partir de uma célula-mãe. Nós estamos falando sobre divisão celular ou “mitose”.
O ciclo celular deve ser regulado. Na verdade, se a divisão celular não for suficiente, o organismo não funcionará de maneira ideal; Por outro lado, se a divisão celular for abundante, as células proliferam de forma descontrolada, o que promove o aparecimento de células cancerosas.
A regulação do ciclo celular é garantida por genes classificados em duas categorias:
- anti-oncogenes que inibem a proliferação celular ao retardar o ciclo celular;
- proto-oncogenes (c-onc) ou oncogenes que promovem a proliferação celular pela ativação do ciclo celular.
Se compararmos o ciclo celular com o do carro, os anti-oncogenes seriam os freios e os proto-oncogenes seriam os aceleradores destes.
Anomalias, patologias ligadas a oncogenes
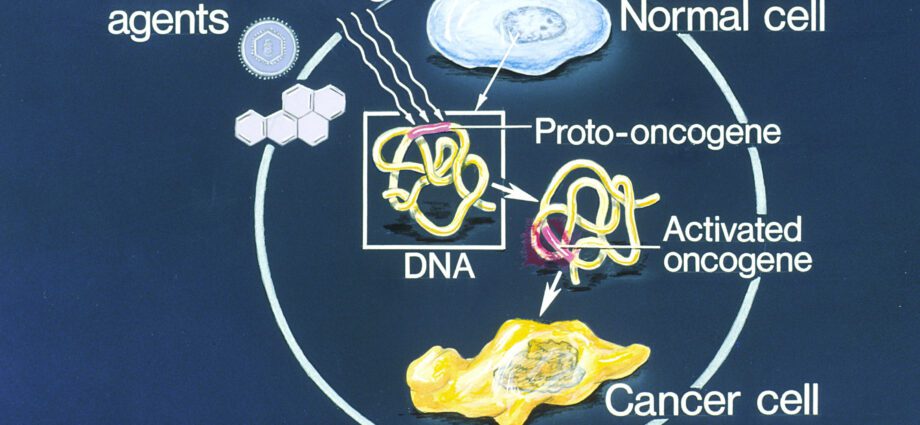
A aparência de um tumor pode resultar de uma mutação que inativa anti-oncogenes ou, ao contrário, de uma mutação que ativa proto-oncogenes (ou oncogenes).
A perda de função dos anti-oncogenes impede que realizem sua atividade inibidora da proliferação celular. A inibição de anti-oncogenes é a porta aberta para a divisão celular descontrolada que pode levar ao aparecimento de células malignas.
No entanto, os anti-oncogenes são genes celulares, ou seja, estão presentes em duplicata no par de cromossomos que os carregam no núcleo da célula. Assim, quando uma cópia do anti-oncogene não é funcional, a outra permite atuar como um freio para que o sujeito fique protegido contra a proliferação celular e contra o risco de tumores. É o caso, por exemplo, do gene BRCA1, cuja mutação inibitória expõe o câncer de mama. Mas se a segunda cópia desse gene é funcional, o paciente permanece protegido, embora esteja predisposto devido à primeira cópia defeituosa. Como parte dessa predisposição, a mastectomia dupla preventiva às vezes é considerada.
Por outro lado, a mutação ativadora que afeta os proto-oncogenes acentua seu efeito estimulante na proliferação celular. Essa proliferação celular anárquica predispõe ao desenvolvimento de cânceres.
Assim como os anti-oncogenes, os pró-oncogenes são genes celulares, presentes em duplicata no par de cromossomos que os carregam. No entanto, ao contrário dos anti-oncongênicos, a presença de um único pró-oncogene mutado é suficiente para produzir os efeitos temidos (neste caso, proliferação celular). O paciente portador dessa mutação está, portanto, em risco de câncer.
Mutações em oncogenes podem ser espontâneas, hereditárias ou mesmo causadas por agentes mutagênicos (produtos químicos, raios ultravioleta, etc.).
Ativação de oncogenes: os mecanismos envolvidos
Vários mecanismos estão na origem das mutações ativadoras de oncogenes ou pró-oncogenes (c-onc):
- integração viral: inserção do vírus DNA ao nível de um gene regulador. É o caso, por exemplo, do papilomavírus humano (HPV), que é transmitido sexualmente;
- mutação pontual em uma sequência de um gene que codifica uma proteína;
- deleção: perda de um fragmento maior ou menor de DNA, constituindo uma causa de mutação genética;
- rearranjo estrutural: alteração cromossômica (translocação, inversão) levando à formação de um gene híbrido que codifica uma proteína não funcional;
- amplificação: multiplicação anormal do número de cópias do gene na célula. Essa amplificação geralmente leva a um aumento no nível de expressão de um gene;
- a desregulação da expressão de um RNA: os genes são desconectados de seu ambiente molecular normal e colocados sob o controle inadequado de outras sequências, causando uma modificação em sua expressão.
Exemplos de oncogenes
Genes que codificam fatores de crescimento ou seus receptores:
- PDGF: codifica o fator de crescimento plaquetário associado ao glioma (um câncer do cérebro);Erb-B: codifica o receptor do fator de crescimento epidérmico. Associado ao glioblastoma (um câncer do cérebro) e câncer de mama;
- Erb-B2 também denominado HER-2 ou neu: codifica um receptor de fator de crescimento. Associado ao câncer de mama, glândula salivar e ovário;
- RET: codifica um receptor de fator de crescimento. Associado ao câncer de tireoide.
Genes que codificam relés citoplasmáticos nas vias de estimulação:
- Ki-ras: associado a câncer de pulmão, ovário, cólon e pâncreas;
- N-ras: associado à leucemia.
Genes que codificam fatores de transcrição que ativam genes promotores de crescimento:
- C-myc: associado a leucemia e câncer de mama, estômago e pulmão;
- N-myc: associado a neuroblastoma (um câncer de células nervosas) e glioblastoma;
- L-myc: associado ao câncer de pulmão.
Genes que codificam outras moléculas:
- Hcl-2: codifica uma proteína que normalmente bloqueia o suicídio celular. Associado a linfomas de linfócitos B;
- Bel-1: também denominado PRAD1. Codifica o Cyclin DXNUMX, um ativador do relógio do ciclo celular. Associado ao câncer de mama, cabeça e pescoço;
- MDM2: codifica um antagonista da proteína produzida pelo gene supressor de tumor.
- P53: associado a sarcomas (cânceres do tecido conjuntivo) e outros cânceres.
Concentre-se nos vírus ocongênicos
Os vírus oncogênicos são vírus que têm a capacidade de tornar cancerígena a célula que infectam. 15% dos cânceres têm uma etiologia viral e esses cânceres virais são a causa de aproximadamente 1.5 milhões de novos casos por ano e 900 mortes por ano em todo o mundo.
Os cânceres virais associados são um problema de saúde pública:
- o papilomavírus está associado a quase 90% dos cânceres cervicais;
- 75% de todos os hepatocarcinomas estão ligados aos vírus da hepatite B e C.
Existem cinco categorias de vírus oncogênicos, sejam eles vírus de RNA ou vírus de DNA.
Vírus RNA
- Retroviridae (HTVL-1) coloca você em risco de leucemia T;
- Flaviviridae (vírus da hepatite C) está sob risco de carcinoma hepatocelular.
Vírus de DNA
- Papovaviridae (papilomavírus 16 e 18) expõe ao câncer do colo do útero;
- Herpesviridae (vírus Esptein Barr) expõe a linfoma B e carcinoma;
- Herpesviridae (herpesvírus humano 8) expõe-se à doença de Kaposi e linfomas;
- Hepadnaviridae (vírus da hepatite B) é suscetível ao carcinoma hepatocelular.